Programa em Urupês oferece tratamento para obesidade no SUS com versões manipuladas de medicamento
A prefeitura de Urupês, município paulista com aproximadamente 14 mil habitantes localizado a 420 quilômetros da capital, anunciou recentemente a implementação de um programa pioneiro que disponibilizará tirzepatida — princípio ativo do medicamento Mounjaro — para o tratamento da obesidade através do Sistema Único de Saúde (SUS). A iniciativa, apresentada como a primeira do estado de São Paulo a oferecer esse tipo de tratamento pela rede pública, tem gerado tanto expectativa quanto preocupação entre especialistas e autoridades sanitárias.
Detalhes do programa e critérios para participação
Segundo informações da administração municipal, o programa tem como objetivo principal atender pacientes em situação de vulnerabilidade social que não possuem condições financeiras para custear o tratamento na rede privada e que estão aguardando na fila para cirurgia bariátrica. A previsão inicial é de que até duzentos pacientes sejam atendidos de forma gradual ao longo da implementação do projeto.
Para participar do programa, os interessados precisam cumprir rigorosos critérios de elegibilidade: ter quarenta anos ou mais; apresentar índice de massa corporal igual ou superior a 35 kg/m² associado a pelo menos uma comorbidade relevante, ou IMC acima de 30 kg/m² com duas comorbidades; além de comprovar tentativa prévia de tratamento não farmacológico para obesidade por no mínimo seis meses. Pacientes com IMC acima de 40 kg/m² estão isentos do critério de idade.
A prefeitura afirma que, além do fornecimento do medicamento, os pacientes selecionados receberão acompanhamento multidisciplinar integral pelo SUS, com equipe composta por endocrinologista, nutricionista, psicólogo, educador físico e assistente social.
Questionamentos sobre segurança e legalidade
Embora a iniciativa pareça promissora à primeira vista, um detalhe crucial tem levantado sérios questionamentos: o medicamento que será fornecido aos pacientes não é o produto original Mounjaro, mas sim versões manipuladas da substância tirzepatida. Esse aspecto fundamental tem gerado debates intensos sobre segurança, qualidade e até mesmo a legalidade do programa.
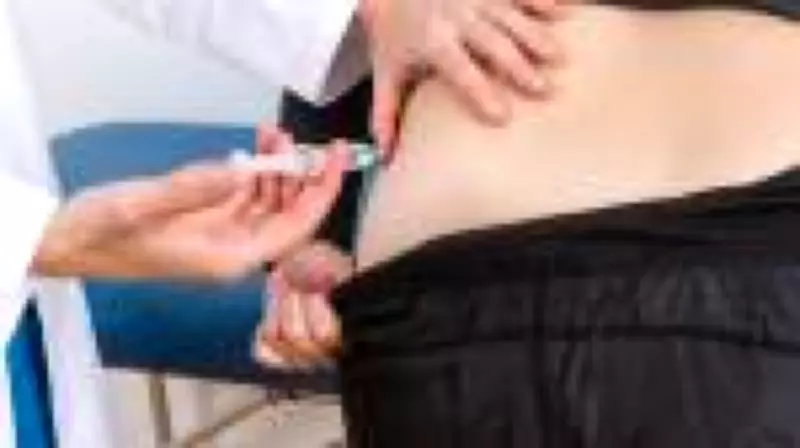
Procurada pela reportagem, a farmacêutica Eli Lilly, responsável pelo desenvolvimento do Mounjaro, afirmou categoricamente que não foi consultada sobre o programa municipal. Além disso, a empresa destacou que, em imagens divulgadas pela prefeitura, o medicamento parece estar sendo aplicado através de seringas convencionais, e não pelas canetas especiais utilizadas no produto original — um forte indício de que se trata efetivamente de formulação manipulada.
Em nota oficial, a companhia declarou estar "profundamente preocupada" com a iniciativa e afirmou que o produto distribuído "não é o Mounjaro". Segundo a Eli Lilly, medicamentos manipulados existem para atender necessidades individualizadas específicas de pacientes quando não há alternativa industrializada disponível, e não para substituir produtos já aprovados pelas agências reguladoras.
"Versões manipuladas em escala industrial não estão sujeitas à aprovação regulatória nem aos controles necessários para síntese, purificação, esterilidade e armazenamento seguros", afirmou a farmacêutica em seu posicionamento.
Riscos sanitários e diferenças regulatórias
Uma das principais preocupações dos especialistas envolve as diferenças regulatórias significativas entre a indústria farmacêutica tradicional e as farmácias de manipulação. Enquanto os fabricantes de medicamentos precisam adquirir insumos farmacêuticos ativos — como a própria tirzepatida — exclusivamente de fornecedores certificados pela Anvisa, submetidos a auditorias rigorosas e inspeções internacionais periódicas, as farmácias magistrais podem importar matérias-primas sem a mesma exigência de certificação e controle de qualidade.
Para Nelson Mussolini, presidente-executivo do Sindicato da Indústria de Produtos Farmacêuticos, esse cenário representa um risco sanitário considerável. "O caso da manipulação dos análogos de GLP-1 configura um risco sanitário intolerável. São moléculas complexas, de produção biotecnológica e altíssima demanda. A indústria farmacêutica investe bilhões em pesquisa e em processos produtivos estéreis para garantir estabilidade e segurança", afirmou o executivo.
A Sociedade Brasileira de Endocrinologia e Metabologia também já emitiu alertas sobre essa prática, destacando que esses estabelecimentos não possuem estrutura adequada para lidar com moléculas biotecnológicas complexas nem o mesmo nível de controle de qualidade das farmacêuticas que desenvolveram os medicamentos originais. De acordo com a entidade, análises laboratoriais já identificaram versões manipuladas com dosagens não estudadas clinicamente e presença de impurezas ou contaminação microbiológica.
Dados de farmacovigilância e notificações
Dados atualizados do sistema de farmacovigilância da Anvisa indicam que, desde 2018, foram registradas 2.436 notificações de eventos adversos supostamente relacionados a medicamentos da classe dos análogos de GLP-1, que inclui semaglutida, liraglutida, dulaglutida e a própria tirzepatida. No mesmo período, houve 65 notificações de mortes suspeitas associadas ao uso dessas canetas injetáveis em todo o território nacional.
A agência reguladora ressalta, contudo, que esses registros possuem limitações importantes. Não é possível determinar com precisão se os casos envolveram medicamentos aprovados oficialmente, versões manipuladas ou produtos completamente irregulares que circulam no mercado paralelo.
A reportagem procurou a prefeitura de Urupês para comentar a iniciativa e os questionamentos levantados, mas não obteve retorno até o momento da publicação deste material. A matéria será atualizada caso haja manifestação oficial por parte da administração municipal sobre os aspectos controversos do programa.









