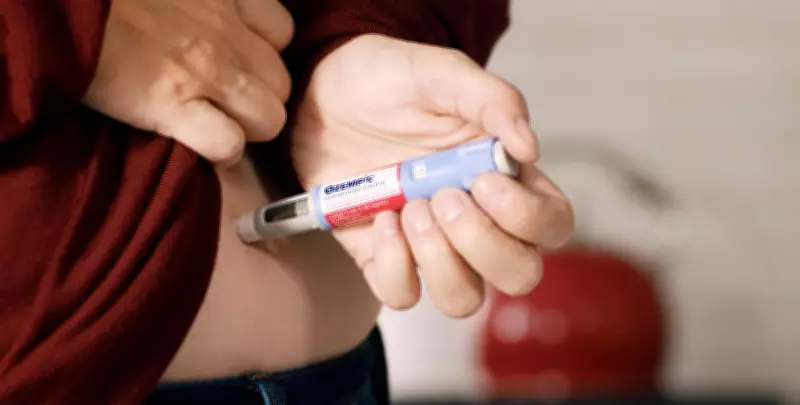
Patente da semaglutida expira, mas versões nacionais do Ozempic ainda não chegam às farmácias
A patente da semaglutida, substância ativa utilizada em medicamentos como o Ozempic, expirou oficialmente nesta sexta-feira (20). A expectativa inicial era de que versões nacionais mais acessíveis chegassem imediatamente às farmácias, porém, essa realidade ainda não se concretizou. Agora, a previsão mais otimista aponta que ao menos uma nova caneta poderá ser aprovada até o mês de junho, após a conclusão da análise técnica pela Agência Nacional de Vigilância Sanitária (Anvisa).
Processo regulatório complexo e demorado
A queda da patente abriu caminho legal para o desenvolvimento de versões mais baratas, mas esse efeito não será imediato devido à complexidade do processo regulatório. Atualmente, existem 15 pedidos nacionais em análise pela Anvisa, e nenhum deles recebeu aprovação definitiva até o momento. A exclusividade da semaglutida pertenceu à farmacêutica Novo Nordisk por duas décadas. A empresa tentou estender esse prazo por mais 12 anos através de ações judiciais, mas não obteve sucesso.
Com o fim da proteção patentária, outras empresas farmacêuticas começaram a investir no desenvolvimento de suas próprias versões do medicamento. No entanto, a chegada dessas alternativas ao mercado depende de um processo regulatório extenso e minucioso. Especialistas explicam que essa demora ocorre devido à natureza complexa da própria substância.
Semaglutida: uma fronteira entre sintético e biológico
A semaglutida é um peptídeo que se situa na fronteira entre os medicamentos sintéticos e os biológicos, o que exige uma análise técnica mais rigorosa e um conjunto ampliado de dados para comprovar segurança e eficácia terapêutica. Dois pedidos encontram-se em fase mais avançada: os das farmacêuticas EMS e Ávita Care. A Anvisa informou que solicitou esclarecimentos adicionais a essas empresas no início de março, e elas dispõem de até 120 dias para responder adequadamente.
Se os dados apresentados forem considerados suficientes e satisfatórios, os produtos poderão finalmente receber a aprovação regulatória. Por esse motivo, a expectativa mais concreta é que ao menos uma dessas versões nacionais comece a ser comercializada nas farmácias brasileiras até o final do primeiro semestre deste ano.
Investimentos milionários e critérios rigorosos
Todo medicamento no Brasil precisa obrigatoriamente passar pela avaliação da Anvisa, que analisa estudos detalhados de segurança e eficácia antes de autorizar a comercialização. No caso específico da semaglutida, esse processo é significativamente mais complexo do que para medicamentos convencionais. Diferentemente de fármacos simples, como a dipirona, que possuem uma composição química bem definida, a semaglutida é uma molécula complexa que pode ser produzida através de diferentes métodos biotecnológicos.
Essa característica impacta diretamente o processo regulatório. O Brasil ainda não possuía uma norma completamente consolidada para esse tipo específico de medicamento, que não se encaixa perfeitamente nas categorias tradicionais. Consequentemente, a Anvisa precisa avaliar cada pedido com base em critérios técnicos diferenciados e referências internacionais, o que torna a análise mais detalhada e, naturalmente, mais demorada.
Os primeiros pedidos de registro começaram a ser protocolados em 2023. Desde então, a agência analisa cada processo individualmente. O cenário atual pode ser resumido da seguinte forma:
- Dois medicamentos estão na fase de cumprimento de exigências técnicas, e o andamento depende diretamente da qualidade e rapidez das respostas das empresas;
- Sete pedidos encontram-se em análise preliminar e devem receber uma primeira decisão, que pode ser uma solicitação de mais esclarecimentos, ainda no primeiro semestre;
- Outros pedidos ainda não tiveram sua análise técnica iniciada pela agência reguladora.
As propostas mais avançadas são das empresas EMS e Ávita Care, que realizaram investimentos bilionários para ingressar nesse mercado promissor. A EMS, por exemplo, investiu aproximadamente R$ 1,2 bilhão na produção nacional da semaglutida, com a expansão de uma unidade industrial em Hortolândia, no interior de São Paulo. A empresa afirma que a nova planta terá capacidade produtiva para fabricar até 20 milhões de canetas por ano.
Raphael Sanches, gerente geral de medicamentos da Anvisa, esclarece que essas duas empresas estão em fase avançada, mas que foram solicitados mais detalhes técnicos para garantir plenamente a segurança da população. "Existem questões de segurança muito delicadas nesses produtos. É por isso que demora. E nós, como a Anvisa, precisamos garantir que nada passe a não ser que cumpra rigorosamente esses critérios", explica o representante da agência.
Etapas finais e questões de segurança
As duas canetas em fase final de análise encontram-se na etapa de esclarecimentos, quando a Anvisa solicita informações adicionais específicas sobre os estudos e os processos de produção apresentados. O foco principal é garantir a segurança absoluta do medicamento e a qualidade consistente do produto final. Entre os principais pontos questionados pela agência estão:
- Estudos de imunogenicidade: avaliam se o organismo do paciente pode produzir anticorpos contra o medicamento, o que poderia fazer com que ele perdesse seu efeito terapêutico ao longo do tempo;
- Controle de impurezas: envolve a identificação e quantificação precisa de resíduos do processo de produção, como solventes e metais, que podem apresentar toxicidade;
- Métodos de análise validados: as empresas precisam comprovar que seus métodos laboratoriais conseguem detectar pequenas variações na molécula da semaglutida e identificar qualquer impureza potencialmente nociva.
As empresas receberam as exigências formais no início de março e possuem até 120 dias corridos para responder — embora possam fazê-lo antes desse prazo. Posteriormente, a Anvisa avaliará se as respostas fornecidas são suficientes e satisfatórias para a concessão da aprovação regulatória. "A Anvisa não é dona total dos prazos. Depende em parte da empresa também, tanto em termos do prazo que a empresa leva para responder quanto em termos da qualidade com a qual ela responde. O quanto isso pode demorar também depende das empresas", complementa Sanches.
Impacto nos preços e no mercado
A queda da patente deve impactar gradualmente os preços dos medicamentos à base de semaglutida, mas esse efeito não será percebido de maneira imediata pelos consumidores. Atualmente, uma caneta de Ozempic, dependendo da dosagem, custa em média R$ 1 mil nas farmácias brasileiras. A redução efetiva dos preços depende da entrada real de concorrentes no mercado farmacêutico — o que ainda não aconteceu no Brasil.
Mesmo assim, a tendência econômica é de que, com o aumento progressivo da concorrência, os valores de mercado sejam pressionados para baixo ao longo do tempo. "Ainda não temos a definição final de preço, mas podemos adiantar que chegaremos de forma competitiva a esse mercado", afirmou Marcus Sanchez, vice-presidente da EMS.
Um dos pontos que complica a questão do preço é que, ao contrário de outros medicamentos convencionais, não haverá versões genéricas tradicionais no mercado. Como a semaglutida é considerada um medicamento biológico, não é tecnicamente possível fabricar cópias idênticas da substância. Um genérico tradicional significaria um custo aproximadamente 35% mais baixo. Em seu lugar, surgirão os chamados medicamentos biossimilares — versões muito semelhantes, mas que exigem testes clínicos próprios para comprovar segurança e eficácia comparáveis. Esses biossimilares podem ser cerca de 20% mais baratos que o produto de referência.
No entanto, entre os pedidos atualmente em análise pela Anvisa, existem apenas dois dessa categoria específica. Os demais são registros de medicamentos novos e, portanto, não possuem qualquer desconto regulatório obrigatório. O fim da exclusividade patentária também não obriga legalmente a Novo Nordisk a reduzir o preço do Ozempic. No entanto, analistas do setor apontam que a empresa poderá adotar estratégias comerciais inteligentes, como programas de descontos e iniciativas de acesso ampliado, para se manter competitiva nesse novo cenário de mercado.
Perspectivas para o Sistema Único de Saúde (SUS)
A possível chegada de versões nacionais da semaglutida também reacende as discussões sobre o uso dessas canetas no Sistema Único de Saúde (SUS). Atualmente, medicamentos dessa classe terapêutica já são utilizados na rede pública de saúde, mas de forma bastante restrita, em protocolos clínicos específicos e para um número limitado de pacientes.
Paralelamente, observa-se um crescimento nas ações judiciais individuais em que pacientes solicitam que o governo forneça esses tratamentos inovadores. Por enquanto, porém, a incorporação formal das canetas de semaglutida no SUS não está prevista no calendário do Ministério da Saúde. No ano passado, a comissão técnica responsável por avaliar a entrada de novos tratamentos na rede pública rejeitou a inclusão da semaglutida. O principal obstáculo identificado foi o custo elevado: estimativas preliminares apontam que a incorporação poderia gerar um gasto adicional de aproximadamente R$ 8 bilhões por ano aos cofres públicos.
O Ministério da Saúde avalia que a queda da patente e a futura entrada de novos concorrentes nacionais podem modificar esse cenário financeiro no médio prazo, ao reduzir progressivamente os preços de aquisição. Ainda assim, não existe, neste momento, nenhuma definição concreta ou previsão oficial de que o medicamento será incorporado à lista de procedimentos do SUS. A discussão permanece em aberto, aguardando desenvolvimentos tanto no campo regulatório quanto no mercado farmacêutico nacional.









