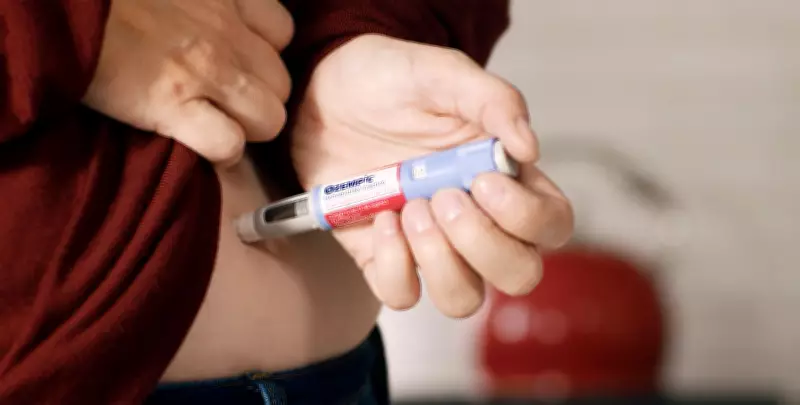
Fim da patente da semaglutida no Brasil abre caminho para concorrência, mas processo será lento
A patente da semaglutida, substância utilizada em medicamentos como o Ozempic para tratamento de diabetes e obesidade, expirou oficialmente no Brasil nesta sexta-feira (20). Após 20 anos de exclusividade da farmacêutica dinamarquesa Novo Nordisk, outras empresas agora podem desenvolver medicamentos à base deste composto, o que teoricamente poderia levar a uma redução de preços no mercado brasileiro.
Contexto brasileiro: obesidade em alta e mercado bilionário
O Brasil enfrenta um cenário preocupante de saúde pública: mais de 60% da população está acima do peso e aproximadamente 25% já apresenta quadros de obesidade. Neste contexto, as canetas injetáveis de semaglutida ganharam popularidade significativa no país, que se tornou o oitavo maior mercado mundial da Novo Nordisk. Somente no ano passado, os produtos à base desta substância movimentaram mais de R$ 12 bilhões em território nacional.
A empresa tentou prolongar sua exclusividade através de ações judiciais que buscavam estender a patente por mais 12 anos, mas não obteve sucesso. Com a queda da proteção patentária, abre-se espaço legal para que empresas brasileiras e estrangeiras desenvolvam suas próprias versões do medicamento.
Processo regulatório: Anvisa tem 14 pedidos em análise
Contudo, o fim da patente não significa que versões alternativas chegarão imediatamente às farmácias. Todas as empresas interessadas precisam passar por um rigoroso processo regulatório junto à Agência Nacional de Vigilância Sanitária (Anvisa). Atualmente, a agência possui 14 pedidos de registro para produção de semaglutida em análise, sendo que apenas três autorizações podem ser concedidas por semestre.
Este trabalho de avaliação deve se estender até meados de 2028, segundo estimativas oficiais. Dois pedidos encontram-se em fase mais avançada: os das farmacêuticas EMS e Ávita Care. A Anvisa havia indicado possibilidade de resposta sobre estes casos ainda nas primeiras semanas de março, mas o prazo não foi cumprido.
Desafios logísticos e classificações especiais
Mesmo após possíveis autorizações, o lançamento de versões nacionais pode enfrentar obstáculos adicionais relacionados à importação de insumos e à distribuição para farmácias em um país de dimensões continentais como o Brasil.
Outro aspecto importante é que nenhuma das versões brasileiras será classificada como medicamento genérico. Por se tratar de um produto biológico (as canetas injetáveis), não existe intercambialidade que caracterize os genéricos tradicionais. Estas versões serão enquadradas como biossimilares, categoria que não exige o desconto mínimo de 35% em relação ao medicamento de referência.
Perspectivas de preço: reduções moderadas
Especialistas do setor farmacêutico indicam que biossimilares costumam apresentar preços cerca de 20% inferiores aos medicamentos biológicos de referência. Aplicando esta estimativa ao cenário atual, onde o Ozempic é vendido por aproximadamente R$ 1.299,70, as versões brasileiras poderiam chegar ao mercado com preços a partir de R$ 1.039,76.
Vale ressaltar que, para estabelecer os preços tanto de similares quanto de biossimilares, são considerados os preços máximos de tabela do medicamento original. Após a queda da patente, a própria Novo Nordisk pode oferecer descontos mais agressivos na tentativa de manter sua participação de mercado, o que poderia pressionar ainda mais os preços dos concorrentes.
Pacientes aguardam definições
No momento, os pacientes que dependem destes medicamentos para tratamento de diabetes e obesidade só terão clareza sobre valores e disponibilidade quando os primeiros produtos forem oficialmente aprovados pela Anvisa. Enquanto isso, o mercado brasileiro de semaglutida permanece dominado pela Novo Nordisk, que continuará comercializando seus produtos até que concorrentes obtenham todas as autorizações necessárias.
O processo ilustra a complexidade da introdução de medicamentos biológicos no mercado brasileiro, mesmo após a expiração de patentes, demonstrando que a tão esperada redução de preços deve ocorrer de forma gradual e moderada nos próximos anos.









